Endometriose: Das unterdiagnostizierte Leiden
Zunehmend erkannt und doch unterdiagnostiziert
2012 wurde die Diagnose Endometriose bei 201.446 Frauen gestellt (standardisierte Diagnoseprävalenz ~0,6%). Ein Jahrzehnt später waren es bereits 339.718 neu diagnostizierte Fälle, was einer standardisierten Diagnoseprävalenz von etwa 1% entspricht. Auswertungen kassenärztlicher Daten zeigen hier eine erfreuliche Entwicklung. Die Autor:innen erklären sich diese mit einem gesteigerten Bewusstsein für die Erkrankung. Dennoch: Die Lebenszeitprävalenz für die Erkrankung liegt bei 11%, was verdeutlicht, dass Endometriose bis heute stark unterdiagnostiziert ist (vgl. Abbildung).[1]
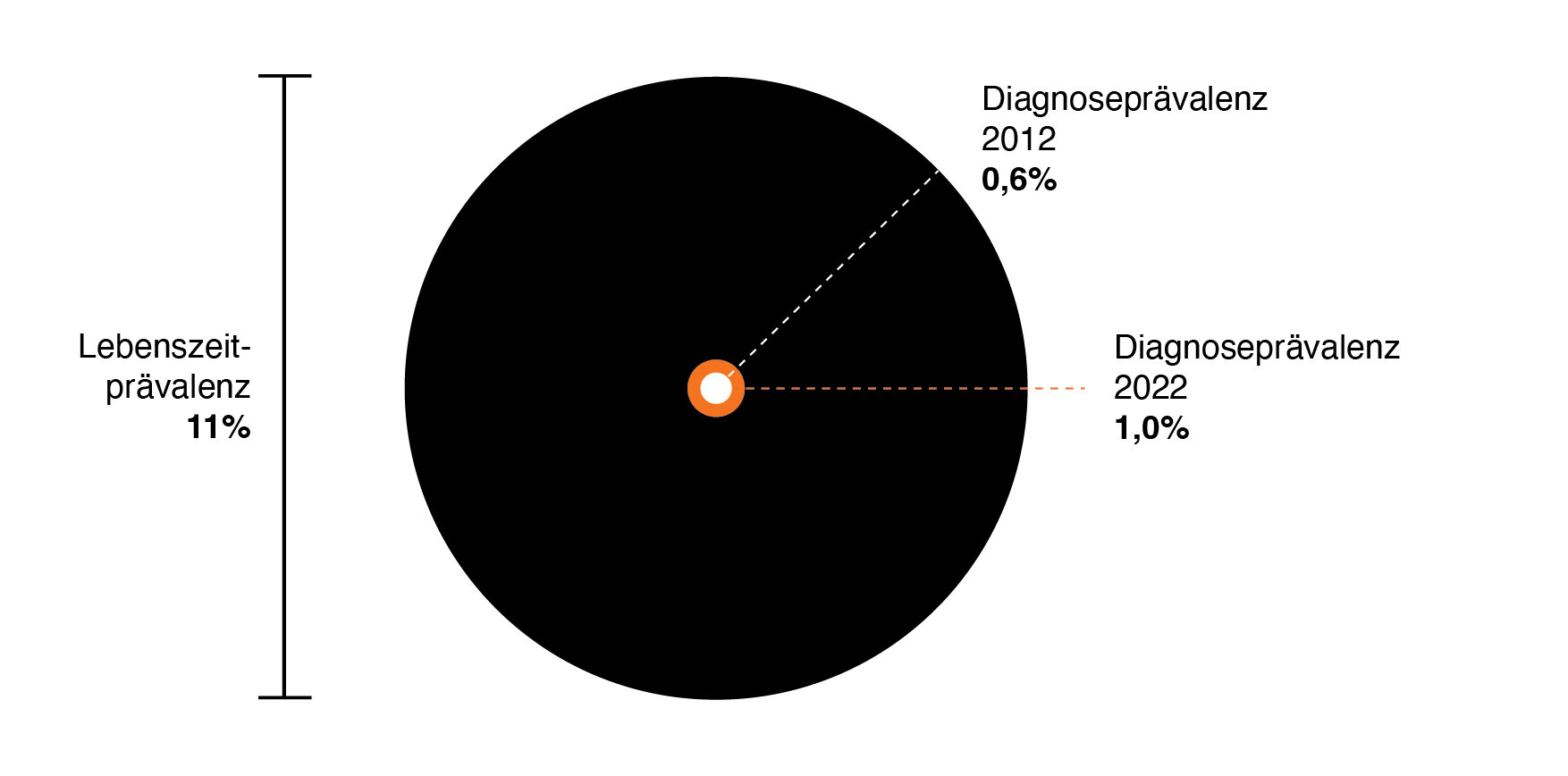
Abbildung: Anstieg der Diagnoseprävalenz zwischen 2012 (weißer Kreis) und 2022 (orangener Kreis) und Vergleich zur Lebenszeitprävalenz (schwarzer Kreis), Angaben aus [1].
Das Chamäleon der Gynäkologie
Zwischen Menarche bis Menopause ist schätzungsweise eine von neun Frauen von Endometriose betroffen.[1] Ätiologie und Pathogenese sind bis heute ungeklärt und die Erkrankung abseits klinisch-intraoperativer Merkmale (s. u.) noch ungenügend charakterisiert.[2,3]
Bei der Endometriose handelt es sich um eine chronische Erkrankung. Krankheitsdefinierend ist die Anwesenheit Endometrium-artigen Epithels und/oder Stroma außerhalb der Gebärmutterhöhle. Endometrioseherde zeichnen sich durch eine komplexe proinflammatorische und endokrine Mikroumgebung aus und werden durch Blut- und Lymphgefäße sowie durch Nerven versorgt.[3,4]
Endometrioseherde können im gesamten Beckenraum auftreten, inklusive Darm, Harnblase und Harnleiter. Herde außerhalb des Beckes, wie z.B. in Lunge, Milz oder im Zwerchfell sowie im Nabelbereich sind selten, aber in der Literatur beschrieben.[2,4]
Die Hauptpräsentationsformen der Endometriose sind:[3]
- Ovarielle Endometriose (auch als Endometriom oder Schokoladenzyste bezeichnet)
- Oberflächliche peritoneale Endometriose
- Tief-infiltrierende Endometriose (mind. 5 mm ins Gewebe reichend), diese Form geht nicht selten auch mit Fibrose und Adhäsion einher
Klinisch kann sich eine Endometriose in einer Myriade verschiedener Symptome äußern, wobei Schmerzen, die bereits ab dem Jugendalter auftreten können, und Fertilitätseinschränkungen Leitsymptome darstellen.
Mögliche Symptome, mit denen sich die Patientin vorstellt, sind unter anderem:
- Chronische Unterleibsschmerzen
- Dysmenorrhö
- Dyspareunie
- Dysurie
- Dyschezie
- Schmerzhafte rektale Blutungen oder Hämaturie während der Menstruation
- Schmerzen in der Schulterspitze
Das Ausmaß der Erkrankung und die Anzahl der Endometrioseherde korrelieren nicht mit Schmerz- und Symptomschwere. Teils bleiben betroffene Frauen auch asymptomatisch und die Endometriose stellt nur einen Zufallsbefund dar,[2] z. B. im Rahmen einer Kinderwunsch- Behandlung.
Abgrenzung zur Adenomyose
Im Gegensatz zur Endometriose bei der Endometrialzellen außerhalb der uterinen Kavität siedeln und wachsen, findet sich bei Adenomyose (auch Adenomyosis uteri) endometriumähnliches Epithel und/oder Stroma in der Muskelschicht der Gebärmutterwand. Teil der histopathologischen Definition ist zudem die Myometrium-Hypertrophie.[5] Trotz einiger Gemeinsamkeiten der Krankheitsbilder werden Endometriose und Adenomyose i. d. R. als separate Entitäten bewertet.[6-8] Die deutsche Leitlinie listet die Adenomyose gegenwärtig als Endometriose-Subform, es bleibt abzuwarten, ob sich dies mit der kommenden Überarbeitung ändern wird.[2]
Die Odyssee der Patientinnen und Diagnosepfade
Bis heute vergehen in Deutschland circa zehn Jahre vom ersten Auftreten Endometriose-bedingter Symptome und der Diagnose.[2] Mögliche Ursachen hierfür sind die komplexe Klinik mit einer Vielzahl möglicher, teils unspezifischer, Symptome, einer immer noch zu geringen Aufklärung über die Erkrankung sowie Stigmata und Verharmlosung bezüglich der Symptome.[3] Der lange Weg bis zur Diagnose begünstigt die Chronifizierung der Symptome. Über die Jahre kann es zum einen zu einer chronischen Entzündung im Bauchraum kommen, begünstigt durch die proinflammatorische Mikroumgebung der Endometrioseherde. Zum anderen ist eine Schmerzsensibilisierung und -ausweitung möglich. In Folge beider Prozesse können schließlich azyklische, chronische Bauchschmerzen auftreten. Diese persistieren teils auch nach Entfernung der Endometrioseherde.[9]
Derzeit findet in der Endometriose-Diagnostik ein Umdenken statt, das in eine schnellere Stellung der Diagnose münden könnte. Technische Fortschritte, insbesondere in der Sonografie, machen die Bildgebung heute zu einem wichtigen Pfeiler in der Diagnostik, während die Bauchspiegelung gezielt bei bestimmten Fragestellungen oder mit dem Ziel der chirurgischen Entfernung eingesetzt wird. Auch die klinisch-anamnestische Diagnosestellung etabliert sich zunehmend, bei einer vermuteten Endometriose geht sie meist mit einem medikamentösen Behandlungsversuch einher.[8]
Einen weiteren Diagnosepfad könnte ein Speicheltest eröffnen, dessen Wiedereinführung auf den deutschen Markt Labor Becker gemeinsam mit DoctorBox begleitet. Um eine Endometriose zu erkennen, wird hier das microRNA-Profil untersucht. In einer Studie mit 200 Patientinnen (153 an Endometriose erkrankt, 47 nicht-erkrankt) zeigten sich hier charakteristische Unterschiede.[10] Der entwickelte Test durchläuft gegenwärtig eine multizentrische Validierungsstudie mit 1.000 eingeschlossenen Patientinnen. Veröffentlichte Interimsergebnisse der ersten 200 Patientinnen konnten die hohe Sensitivität und Spezifität des Tests (jeweils >95%) bestätigen.[11] Klinischen Mehrwert könnte der nicht-invasive Biomarker-basierte Test insbesondere aufgrund der schnellen Diagnosestellung bieten. Binnen weniger Wochen liegt ein positiv- bzw. negativ-Ergebnis vor.
Tab. 1: Optionen in der Endometriose-Diagnostik im Überblick
| Methode | Laparoskopie | Bildgebung (Ultraschall u/o MRT) | Klinisch-anamnestische Diagnosestellung | Speicheltest |
| Klinische Bedeutung |
|
|
|
|
| Limitationen |
|
|
|
|
Fazit
Ein Umdenken und neue diagnostische Optionen in der Endometriose-Diagnostik lassen darauf hoffen, dass der Weg zur Diagnose in Zukunft für die Patientinnen keiner Odysee mehr gleichen muss und dass die Endometriose keine unterdiagnostizierte Erkrankung bleibt.
Referenzen
[1] Kohring C et al. Endometriose in der vertragsärztlichen Versorgung – Regionale und zeitliche Trends im Zeitraum 2012 bis 2022. Zentralinstitut für die kassenärztliche Versorgung in Deutschland (Zi). Versorgungsatlas-Bericht Nr. 24/01. Berlin 2024.
[2] AWMF-Leitlinie. S2k-Leitlinie Diagnostik und Therapie der Endometriose. AWMF 2020. Version 1.0. Aufgerufen unter https://register.awmf.org/assets/guidelines/015-045l_S2k_Diagnostik_Therapie_Endometriose_2020-09.pdf, aufgerufen am 02.05.2024
[3] Zondervan K T et al. Endometriosis. The New England Journal of Medicine 2020;382(13):1244-1256.
[4] Gülden H et al. Diagnose und Therapie der tief-infiltrierenden Endometriose. Dtsch Arztebl Int 2010;107(25): 446-55.
[5] Zaloudek C, Norris H J. Mesenchymal tumors of the uterus. In: Kurmann R.J. Blaunstein’s Pathology of the Female Genital Tract. 3rd ed. Springer-Verlag, New York, NY1987: 374.
[6] Benagiano G et al. Structural and molecular features of the endomyometrium in endometriosis and adenomyosis. Hum Reprod Update. 2014;20(3):386-402.
[7] Vannuccini S et al. Pathogenesis of adenomyosis: an update on molecular mechanisms. Reprod Biomed Online 2017;35(5):592-601.
[8] Becker C M et al. ESHRE guideline: endometriosis. Hum Reprod Open 2022;2022(2):hoac009
[9] Grabherr R. Endometriose als diagnostische Herausforderung. Universimed 2019. Aufgerufen über: https://www.universimed.com/ch/article/gynaekologie-geburtshilfe/endometriose-als-diagnostische-herausforderung-2118958, aufgerufen am: 03.05.2024
[10] Bendifallah S et al. Salivary MicroRNA Signature for Diagnosis of Endometriosis. J Clin Med. 2022;11(3):612.
[11] Bendifallah S et al. Validation of a Salivary miRNA Signature of Endometriosis — Interim Data. NEJM Evidence 2023;2(7):EVIDoa2200282.